بررسی ساختاری ZrO2 پایدارشده در نمونههای کامپوزیت –Al2O3-ZrO2α
سلهای سوختی جامد اکسیدی در بسیار موارد در صنایع مختلف وجود دارند. صنایع خودروسازی، نیروگاههای برق، هوافضا و سایر صنایع، نمونههایی از این کاربردها هستند. به دلیل مصارف زیاد این سلها در صنایع، بهکارگیری موادی که فرآیندها را سادهتر و سریعتر سازد، ضرورت دارد. کامپوزیت α-Al2O3-ZrO2، مواد رسانای بسیار قوی آنیونی است که در دماهای بالا نیز بهخوبی عمل میکند. بنابراین از این ترکیب به عنوان الکترولیت در کاربردهای سل های سوختی جامد استفاده میشود. این کامپوزیتها ضریب حرارتی بالایی دارند و در برابر شوک حرارتی، مقاوم هستند. تقویتکردن بستر زیرکونیا با آلفاآلومینا، توان کششی و توان حرارتی را ارتقا میدهد، در حالی که وزن بستر جامد، بسیار سبک خواهد بود.
فاز تتراگونال ZrO2 معمولا در بالای 1473 کلوین پایدار است. در دماهای کمتر از 1473 کلوین، از طریق دوپینگ با کاتیونهای مناسب پایدار میشود. این کاتیونها شامل Y3+، Ca2+، Ce4+، Mg2+ و غیره هستند که بهطور تصادفی مکان Zr را اشغال میکنند، در حالی که تعادل شارژ با تعداد مناسبی از جای خالی در مکانهای O بهدست میآید. مکانیسمهای دیگری مانند کنترل اندازه کریستالیت (گاروی، 1978)، میکرواسترین (فاغرازی و همکاران، 1980؛ میتسوهشی و همکاران، 1974) یا جای خالی اکسیژن در t-ZrO2 خالص (فابریس و همکارانش، 2002) نیز برای تثبیت فاز t-ZrO2 در دمای اتاق شناخته شدهاند. یاشیما و همکارانش در سال 2006 نشان دادند که نانوذرات t-ZrO2 در واقع یک فاز کمبود اکسیژن هستند.
خواص مکانیکی سرامیک آلومینا را میتوان بهطور قابلتوجهی با بهکاربردن ذرات ریز ZrO2 افزایش داد. در پژوهشی که توسط کانتی دب و همکارانش در سال 2006 انجام شد، پودرهای کامپوزیت α-Al2O3-ZrO2 با روش احتراق تهیه شدند. مشاهده شد که ذرات t-ZrO2 پایدارشده را میتوان در داخل منافذ دانههای α-Al2O3 رشد داد. برای کامپوزیتهای با مقدار α-Al2O3 (30 درصد وزنی)، یک تبدیل ساختاری برای ZrO2 از تتراگونال به مونوکلینیک هنگام آنیل نمونه در 1473 کلوین، مشاهده شده است. مقدار اندازه بحرانی 54 نانومتر و میکروکرنش 3-10×5/2 به پایداری فاز تتراگونال ZrO2 نسبت داده شد. در مطالعه حاضر، کانتی دب و همکارانش در سال 2006 در هند، قابلیت دوام و ماندگاری سایر مکانیسمهای پایداری را در نمونههای کامپوزیت α-Al2O3-ZrO2 مورد بررسی قرار دادهاند.
دو کامپوزیت با ترکیبات وزن اسمی اولیه (Al2O3:t-ZrO2-α)، 63:35 و 29:58 درصد وزنی، با روش احتراق از نیترات آلومینیوم و زیرکونیل نیترات تجاری موجود و اوره تهیه شدهاند که به عنوان نمونههای 1 و 2 نامیده میشوند. سپس نمونهها در 1473 درجه کلوین آنیل شده و مورد آنالیزهای مختلف قرار گرفتهاند.
شرح نتایج
شکل 1 الگوهای پراش پرتو ایکس پودرهای کامپوزیت α-Al2O3-ZrO2 فاقد آنیل و آنیلشده را نشان میدهد.
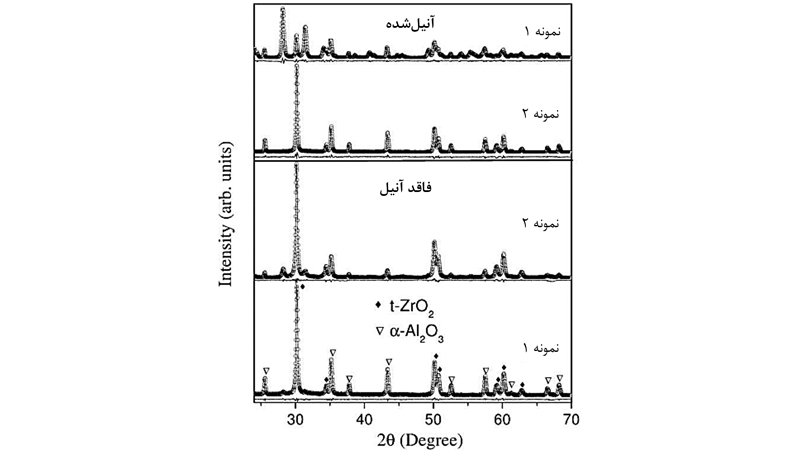
شکل1. الگوهای پراش پرتو ایکس نمونههای کامپوزیت α-Al2O3-ZrO2 فاقد آنیل و آنیلشده.
بر اساس روش ریتولد، نمونه فاقد آنیل 1، دارای فاز اصلی تتراگونال ZrO2، حدود 36 درصد وزنی است، در حالی که برای نمونه 2، علاوه بر t-ZrO2، فاز مونوکلینیک m-ZrO2 با کسر وزنی حدود 12 درصد وزنی نیز وجود دارد. مقدار اعوجاج تتراگونال، 052/0 برای هر دو نمونه است. مقدار اعوجاج این دو نمونه با مقدار اعواج t-ZrO2 خالص (05/0=δ) و t-ZrO2 پایدارشده با اندازه (047/0=δ )، مطابقت دارد. برای فاز t-ZrO2 پایدارشده توسط دوپینگ کاتیونی، مقدار اعوجاج تتراگونال تابعی از غلظت کاتیون است. برای نمونههای کامپوزیت α-Al2O3-ZrO2 حاضر، هیچ تغییر قابلاندازهگیری در اعوجاج تتراگونال وجود ندارد، که نشان میدهد یونهای Al+3جایگزین یونهای Zr+4 در شبکه ZrO2 نمیشوند. با این حال، گزارش شده است که وقتی کامپوزیتهای α-Al2O3-t-ZrO2 به روش سنتز درجا تهیه میشوند، احتمال دوپینگ Al+3 وجود دارد. اما در مورد حاضر نمیتوان آن را ثابت کرد. شعاع یونی Al+3 با عدد همسایگی هشت، 68/0 آنگستروم است که در مقایسه با شعاع یونی Zr+4 (84/0 آنگستروم) با عدد همسایگی هشت، بسیار کمتر است، که نشان میدهد ZrO2 دوپشده با Al+3 ممکن است پایدار نباشد.
از جدول 1 بیشتر مشهود است که اعوجاج تتراگونال نیز مستقل از مقدار -Al2O3α برای نمونههای کامپوزیت α-Al2O3-ZrO2 آنیلشده است. با این حال پس از آنیل، درصد وزنی t-ZrO2 تقریبا برای نمونه 1 ثابت میماند، اما برای نمونه 2، درصد وزنی m-ZrO2 به 50 درصد وزنی افزایش مییابد. این نشان میدهد که پس از آنیل، یک تبدیل جزئی از t-ZrO2 به m-ZrO2 وجود دارد. بنابراین واضح است که فاز تتراگونال ZrO2 در زمینه -Al2O3α به دلیل دوپینگ کاتیونی پایدار نشده است.
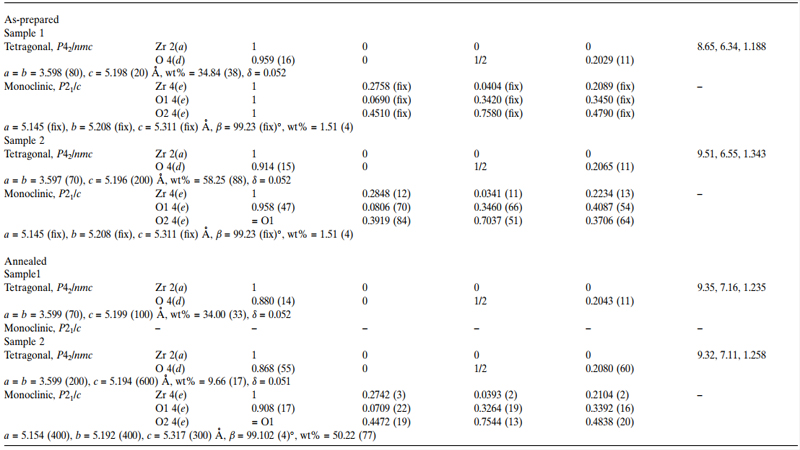
جدول1. پارامترهای ساختار کریستالی اصلاحشده و فاکتورهای حاصل از آنالیز ریتولد برای فازهای زیرکونیا در نمونههای کامپوزیت α-Al2O3-ZrO2 فاقد آنیل و آنیلشده
طیف FTIR هر دو نمونه کامپوزیت α-Al2O3-ZrO2 فاقد آنیل و آنیلشده در شکل 2 نشان داده شده است. طیف FTIR، پیکهای جذب معمولی α-Al2O3، t-ZrO2 و m-ZrO2 را نشان میدهد. پیکهای مشخصه برای محلول جامد ZrO2-Al2O3، که در حدود 434، 448 و 460 سانتیمتر مربع ظاهر میشوند، وجود ندارند. بنابراین، میتوانیم از تجزیه و تحلیل FTIR نتیجه بگیریم که تشکیل محلول جامد رخ نمیدهد. با این حال، وجود جای خالی اکسیژن را نمیتوان رد کرد. در اینجا میتوان به این نکته اشاره کرد که اگرچه فضای خالی اکسیژن برای تثبیت فاز مکعبی مورد نیاز است، اما منجر به فاز تتراگونال دوپشده پایدار نمیشود.
در جدول 1 همچنین مقادیر جابجایی z از اتم O ذکر شده است. برای نمونه فاقد آنیل، جابجایی z مستقل از مقدار α-Al2O3 است و با مقدار یک ساختار تتراگونال ایدهآل مطابقت دارد. با این حال، برای نمونه آنیلشده 2، مقدار z کمی بالاتر است.
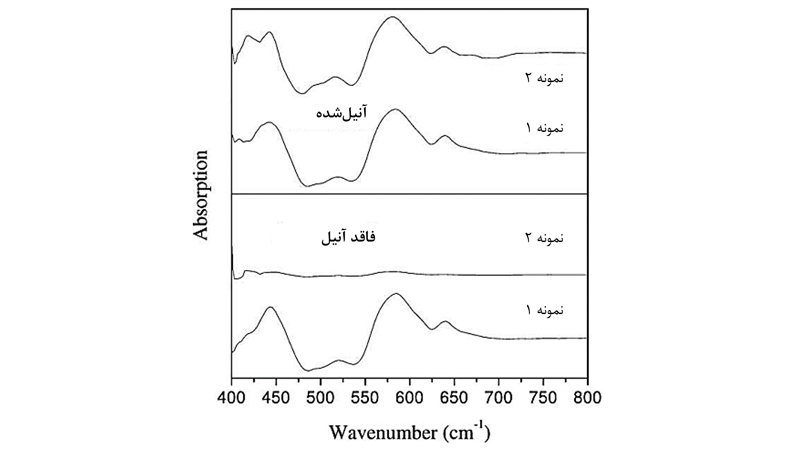
شکل2. طیف FTIR نمونههای کامپوزیت α-Al2O3-ZrO2 فاقد آنیل و آنیلشده.
جدول 2 نشاندهنده طول پیوند Zr-O وZr-Zr بهدست آمده از پارامترهای ساختاری اصلاح شده نمونههای کامپوزیت α-Al2O3-ZrO2 فاقد آنیل و آنیلشده است. برای نمونههای فاقد آنیل، تفاوت کمی بین دو طول پیوند Zr-Zr وجود دارد که نشان میدهد زیرشبکه Zr دارای اعوجاج جزئی است. میانگین طول پیوند، 617/3 آنگستروم و تقریبا برابر با ساختار ایدهآل فاز تتراگونالZrO2 (62/3 آنگستروم) است. طول پیوند Zr-O برای نمونه فاقد آنیل 1، 085/2 و 371/2 آنگستروم با مقدار میانگین 23/2 آنگستروم است و مشابه مقداری است که برای ZrO2 دوپشده با Y بهدست آمده است. آنیل در 1473 کلوین، منجر به تفاوت قابلتوجهی در مقدار میانگین طول پیوند نمیشود. با این حال، آنیل یک تغییر جزئی در طول پیوند Zr-Zr ایجاد میکند و یک شبکه کاتیونی تقریبا کامل fcc ایجاد میشود. میانگین طول پیوند Zr-O برای نمونههای کامپوزیت α-Al2O3-ZrO2 فاقد آنیل و آنیلشده 2، مشابه است. نتایج همچنین مطابق با نتایج طیفسنجی جذب پرتو ایکس (EXAFS) برای t-ZrO2 دوپشده با کاتیونهای مختلف است. علیرغم این واقعیت که میانگین طول پیوند Zr-O یکسان است، مقدار طول پیوند برای نمونه فاقد آنیل 2، تغییراتی را نسبت به نتایج دیگر نشان میدهد که نشاندهنده مقدار متفاوتی از اعوجاج شبکه O است. این تغییر موضعی ممکن است باعث تبدیل m-ZrO2 t→ نمونه 2 پس از آنیل شده باشد.
ضریب اشغال اتمهای O فازهای تتراگونال و مونوکلینیک هرکدام بهطور مستقل اصلاح شدند. برای فاز تتراگونال ZrO2 در نمونه 1، این فاکتور به 96/0 اصلاح شد، که پس از آنیل به 88/0 کاهش یافت. این نشان میدهد که فاز تتراگونال در واقع یک شکل کمبود اکسیژن ZrO2-x است که x از 08/0 تا 24/0 متغیر است. همچنین مشاهده شد که فاز m-ZrO2 نیز با ضریب اشغال به 93/0 دچار کمبود اکسیژن است و تقریبا پس از آنیل بدون تغییر باقی میماند. نتایج فوق نشان میدهد که جای خالی اکسیژن نقش مهمی در تثبیت فاز تتراگونال ایفا میکند و تبدیل تتراگونال به مونوکلینیک در واقع با کمبود اکسیژن مرتبط است.
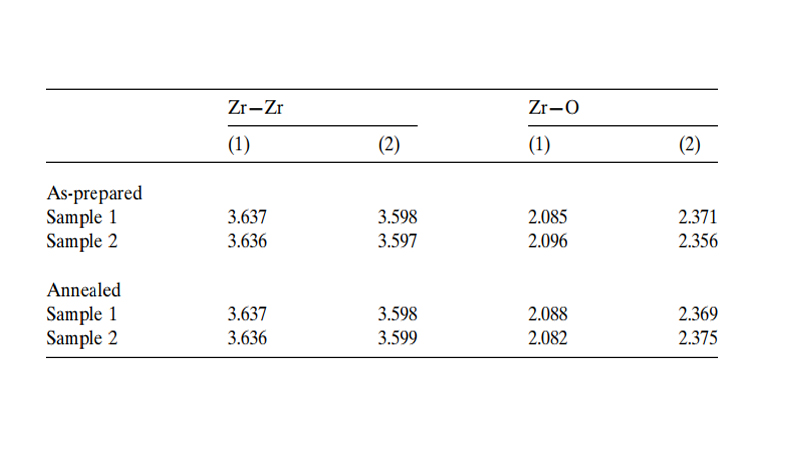
جدول2. طول پیوند برای نمونههای کامپوزیت α-Al2O3-ZrO2 فاقد آنیل و آنیلشده