ویژگیهای ساختاری اکسید زیرکونیوم
اکسید زیرکونیوم با نقطه ذوب حدود 2700 درجه سانتیگراد و مقاومت شیمیایی کمنظیر، در صنعت سرامیک دارای اهمیت فراوانی است. این ماده دارای سه شکل پلیمورفیک است که عبارتند از: مونوکلینیک، تتراگونال و مکعبی. زیرکونیا در دمای اتاق دارای ساختار مونوکلینیک است که با افزایش دما به بیش از 1170 درجه سانتیگراد ساختار آن به تتراگونال تغییر میکند. با انتقال از فاز مونوکلینیک به تتراگونال، یک انقباض حدود 10 – 5 درصد حجمی اتفاق میافتد. با بالارفتن دما، انتقال فاز تتراگونال به مکعبی در دمای 2350 درجه سانتگراد رخ میدهد و درنهایت این اکسید در 2700 درجه سانتیگراد ذوب میشود.
بررسی ساختاری اکسید زیرکونیوم
فاز مونوکلینیک اکسید زیرکونیوم
شکل طبیعی اکسید زیرکونیوم که با نام بادلیت شناخته میشود، حاوی حدود 2 درصد اکسید هافنیوم (HfO2) است اما اثر آن بر خواص ساختاری و شیمیایی این ماده بسیار کم است. پارامترهای سلول واحد مونوکلینیک برابر است با: nm 5169/0 = a، nm 5232/0 = b و nm 5341/0 = c. یونهای Zr4- در همسایگی هفت عدد یون اکسیژن قرار دارند که در مکانهای تتراهدرال جای گرفتهاند که فاصلخ متوسط بین سه اکسیژن و یون زیرکونیوم، Å 07/2 است و چهار یون دیگر اکسیژن در فاصله Å 21/2 قرار گرفتهاند. ساختار اکسید زیرکونیوم مونوکلینیک در شکل 1 نشان داده شده است.
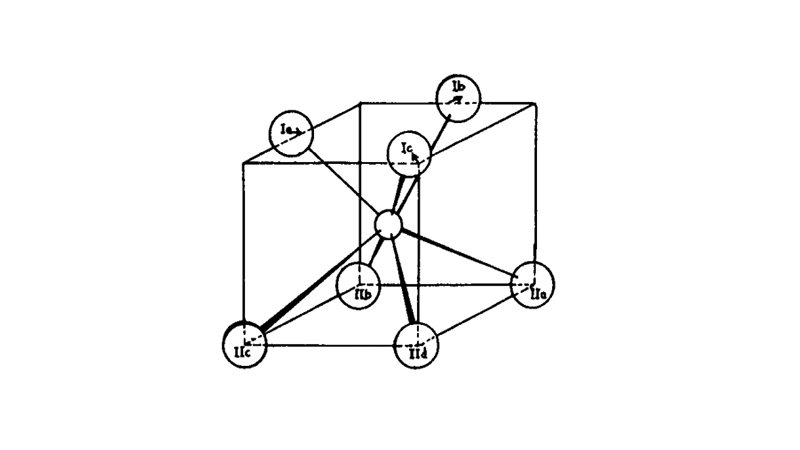
شکل1. ساختار فاز مونوکلینیک اکسید زیرکونیوم.
این همسایگی با زاویه 3/134 است که با زاویه 5/109 مکان تتراهدرال کمی اختلاف دارد. بنابراین ساختار یونهای اکسیژن مسطح نیست، درنتیجه یک خمیدگی در صفحه چهار یون اکسیژن ایجاد میشود و همچنین باعث بینظمی کامل در صفحه سه اکسیژن دیگر میشود. مطابق شکل فوق، سه اکسیژن به صورت کاملا نامنظم در ساختار قرار گرفتهاند. نتیجه این نامنظمی، تمایل به انجام دوقلویی است. صفحه دوقلویی (010) از یونهای װO تشکیل شده است که باعث میشود یونهای موجود در صفحه دوقلویی کمی از وضعیت تعادلی خود خارج شوند به نحوی که حداقل تغییر شکل صورت میگیرد. این تغییر شکل، در شکل2 نشان داده شده است. همچنین اطلاعات کریستالوگرافی کلی اکسید زیرکونیوم در جدول 1 آورده شده است.
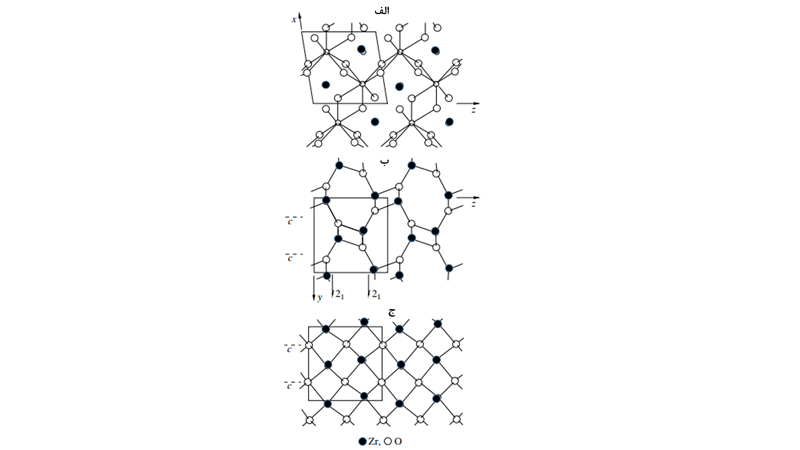
شکل2. الف) ساختار فاز مونوکلینیک اکسید زیرکونیوم در صفحه (010) ب) چرخش ساختار زیرکونیای مونوکلینیک در فضای سه بعدی ج) ساختار زیرکونیای مونوکلینیک در صفحه (100).

جدول1. اطلاعات کریستالوگرافی کلی اکسید زیرکونیوم با فاز مونوکلینیک
فاز تتراگونال اکسید زیرکونیوم
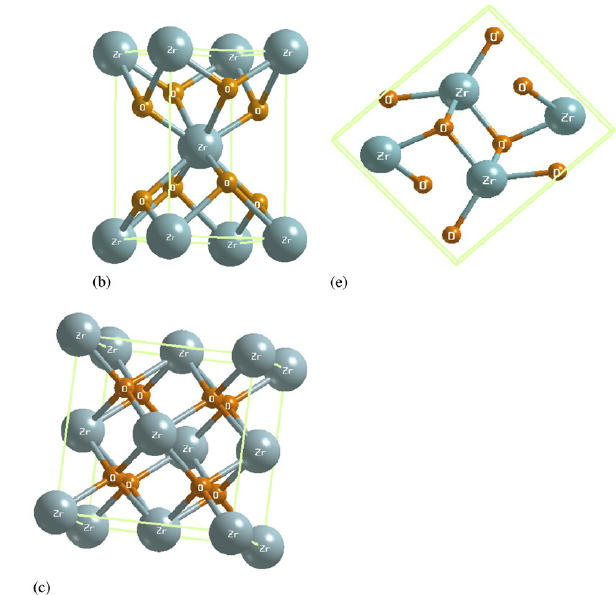
اکسید زیرکونیوم با فاز تتراگونال یک بلور عمودی مستطیلشکل است. یون Zr4+ در این فاز دارای عدد همسایگی هشت هستند. در این حالت یک تغییر شکل ناشی از قرارگیری چهار یون اکسیژن در فاصله Å 065/2 به صورت یک تتراهدرال مسطح و چهار اکسیژن دیگر در فاصله Å 455/2 در یک تتراهدرال کشیده که حدود 90 درجه چرخیده است، رخ میدهد. این ساختار در شکل 3 نشان داده شده است. دو یون زیرکونیوم ساختار تتراگونال در مکانهای (0، 0، 0) و (2/1، 2/1، 2/1) قرار دارند. همچنین چهار یون اکسیژن در مکانهای (Z، 2/1، 0)، (-Z، 0، 2/1)، (Z+2/1، 2/1، 0) و (Z-2/1، 0، 2/1) قرار دارند که 185/0 = Z است. در شکل 4 چیدمان اتمها به ترتیب در صفحات (110) و (001) نشان داده شده است. همچنین اطلاعات کریستالوگرافی کلی اکسید زیرکونیوم با فاز تتراگونال در جدول 2 آورده شده است.
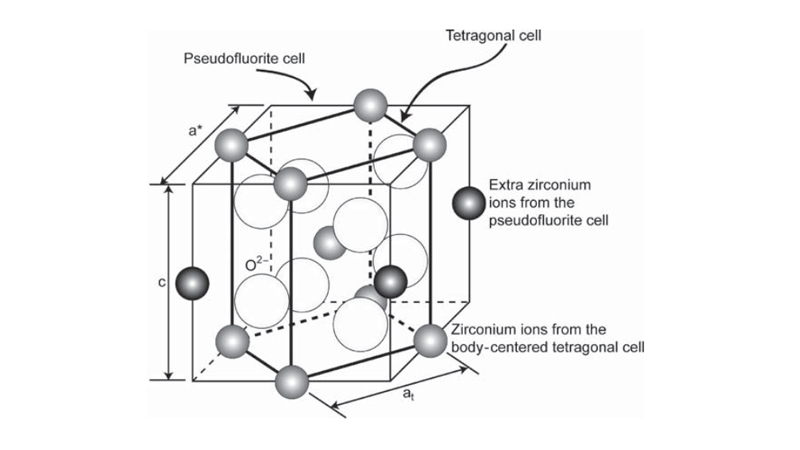
شکل3. ساختار فاز تتراگونال اکسید زیرکونیوم.
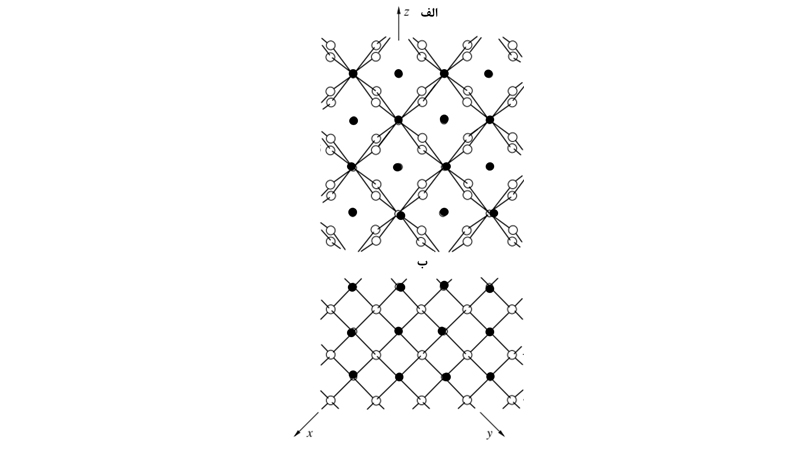
شکل4. ساختار فاز تتراگونال اکسید زیرکونیوم در صفحه (110) ب) ساختار فاز تتراگونال اکسید زیرکونیوم در صفحه (001).

جدول2. اطلاعات کریستالوگرافی کلی اکسید زیرکونیوم با فاز تتراگونال
فاز مکعبی اکسید زیرکونیوم
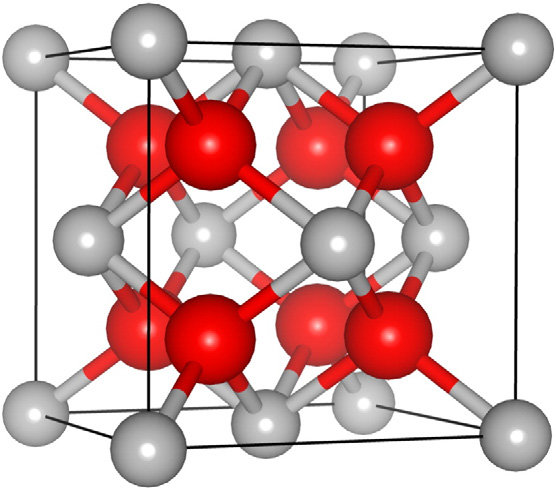
اکسید زیرکونیوم با فاز مکعبی دارای ساختاری با وجوه مرکزدار (FCC) با ساختاری معروف به فلوریت که یونهای Zr4+ در مکانهای FCC قرار دارند . هشت یون O2- در مکانهای تتراهدرال و به صورت کاملا متقارن قرار گرفتهاند. ساختار زیرکونیا با فاز مکعبی در شکل 5 نشان داده شده است.
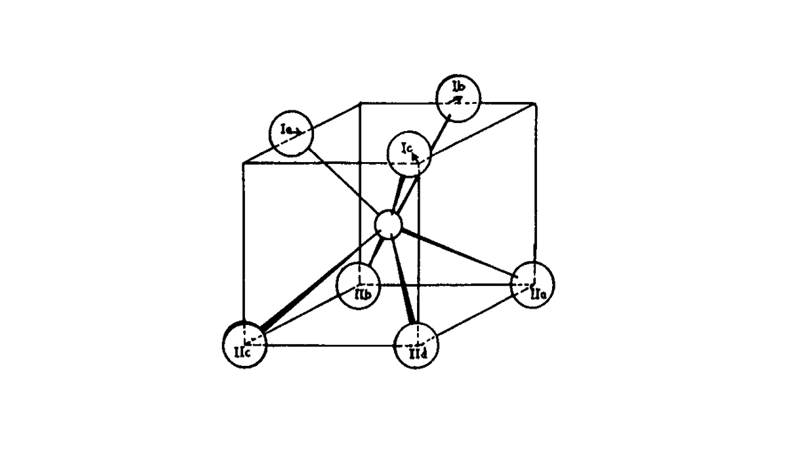
شکل5. ساختار فاز مکعبی اکسید زیرکونیوم.
یونهای Zr4+ در مکانهای (0، 0، 0)، (2/1، 2/1، 2/1)، (2/1، 0، 2/1) و ( 2/1، 2/1، 0) و همچنین یونهای O2- در مکانهای (4/1، 4/1، 4/1)، (4/3، 4/1، 4/1)، (4/1، 4/3، 4/1)، (4/1، 4/1، 4/3)، (4/1، 4/3، 4/3)، (4/3، 4/1، 4/3)، (4/3، 4/3، 4/1)، (4/3، 4/3، 4/3) قرار دارند. همچنین بردار انتقال برای ساختار مکعبی عبارتند از: (2/a، 2/a، 0)=t1، (2/a، 0، 2/a)=t2 و (0، 2/a، 2/a)=t3. همچنین اطلاعات کریستالوگرافی کلی اکسید زیرکونیوم با فاز مکعبی در جدول 3 آورده شده است.
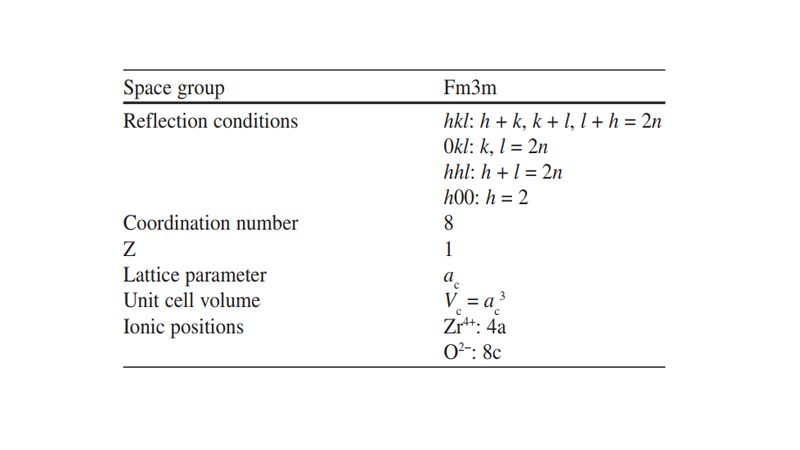
شکل5. ساختار فاز مکعبی اکسید زیرکونیوم.
استحاله فازی در اکسید زیرکونیوم
دو نوع انتقال غیرنفوذی در سرامیکها وجود دارد. انتقال بازسازی و انتقال جانشینی. انتقال بازسازی شامل خرابی و بازسازی پیوندهای یونی و کوالانت است که با یک نیروی زیاد برای انتقال به وجود میآید. انتقال جانشینی شامل عدم خرابی پیوندها در درون فاز است. تغییر مکان نسبی شبکه کریستال در صفحات کریستالوگرافی معین برای انتقال جانشینی صورت میگیرد که این اتقال خیلی سادهتر از انتقال بازسازی انجام میشود.
انتقال غیرنفوذی تتراگونال به مونوکلینیک اکسید زیرکونیوم، غلبه بر تغییر مکان نسبی یونهای سازنده است که این انتقال غیرنفوذی را مارتنزیت مینامند. انتقال تتراگونال به مونوکلینیک زیرکونیا، برای اولینبار توسط راف و ابرت در سال 1929 به وسیله آزمایش XRD دمابالا کشف شد.
گاروی بر اساس کار انجامشده با استفاده از کریستال منفرد کرنشنیافته، نتیجه گرفت که تبدیل مونوکلینیک به تتراگونال از نظر ترمودینامیکی برگشتپذیر است. انتقال فاز تتراگونال به مونوکلینیک پودرهای زیرکونیا، بر اساس فرآیند برشی بدون نفوذ صورت میگیرد. سرعت انتقال فاز تتراگونال به مونوکلینیک به سرعت تشکیل مارتنزیت در فولادها تشبیه شده است.
این انتقال در حالت رفت در دمای 6 ± 1174 درجه سانتیگراد و در حالت برگشت در دمای 950 درجه سانتیگراد صورت میگیرد. انتقال فاز مونوکلینیک به تتراگونال و برعکس که بهترتیب با گرمکردن و سردکردن پودر صورت میگیرد، باعث تشکیل یک هیسترزیس حرارتی میشود. انتقال مارتنزیت تتراگونال به مونوکلینیک اکسید زیرکونیوم همراه با هیسترزیس حرارتی در محدوده 300 – 150 کلوین صورت میگیرد.
این هیسترزیس به فاکتورهای مختلفی بستگی دارد که به صورت قطعی ثابت نشدهاند. منحنیهای هیسترزیس حرارتی بهطور کلی برای تعیین دماهای شروع مارتنزیت (Ms) و شروع آستنیت (As) و همچنین دمای ( T0) مونوکلینیک و تتراگونال زیرکونیا که انرژی آزاد مشابهی دارند، استفاده میشود. دمای انتقال به اندازه ذرات نیز بستگی دارد. ذرات ریزتر زیرکونیا نسبت به ذرات درشتتر، در دمای پایینتری تبدیل میشوند.
اما انتقال تتراگونال به مونوکلینیک با افزایش 5 – 3 درصد حجمی همراه است که این افزایش حجم باعث ایجاد تنش و شکست در ساختار اکسید زیرکونیوم میشود. انتقال فاز تتراگونال به مکعبی و برعکس نیز، بدون نفوذ صورت میگیرد و این اتفاق با متقارنشدن ساختار در هنگام تبدیل فاز تتراگونال به مکعبی همراه است. همچنین این انتقال همراه با تغییر شکل دوقلویی است.